او به آلزایمر زودرس مبتلا نشد. آیا یک جهش نادر از او محافظت کرده بود

قرار بر این بود که او به آلزایمر زودرس مبتلا شود، اما این اتفاق نیفتاد. آیا یک جهش نادر از او محافظت کرده بود؟
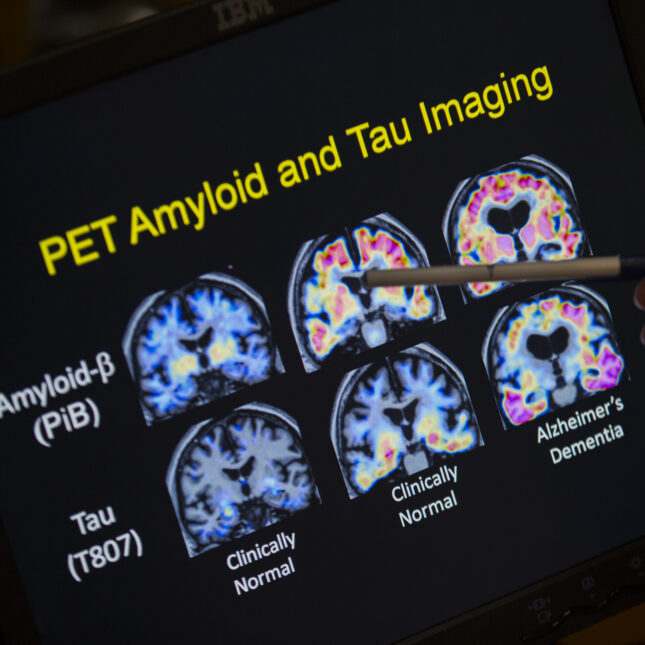
تصویربرداری از تاو آلزایمر
یک زن دارای جهش ژنتیکی که پیش بینی شده بود در دهه پنجم زندگیش (پنجاه سالگی) به بیماری آلزایمر مبتلا خواهد شد توانست از سرنوشت خودش فرار کند و قبل از اینکه به زوال عقل خفیف مبتلا شود تا ۷۰ سالگی زندگی کند – محققان فکر میکنند علت این امر را بدانند.
آنها در روز دوشنبه گزارش کردند که او علاوه بر جهش آلزایمر دارای شکل نادری از یک ژن است که به دلیل تولید مولکولهایی که به انتقال کلسترول از طریق جریان خون کمک میکند، به خوبی آن را میشناسیم. ژن دوم به نحوی از پیامدهای مخرب ژن اول جلوگیری کرده بود و این یافتهای است که میتواند رویکردهای جدیدی را برای درمان یا پیشگیری از آلزایمر پیش رویمان بگذارد.
دکتر مایکل گریسیوس، متخصص ژنتیک آلزایمر از دانشکده پزشکی استنفورد که در این پژوهش شرکت نداشت گفت، این یک تحقیق عالی و قابل تامل میباشد. با این حال او تاکید کرد که از آن جا که ترکیب ژنهای این بیمار بسیار غیر معمول و منحصر به فرد میباشد، از این رو این فرضیه نمیتواند قطعی باشد – این مطالعه در Nature Medicine منتشر گردیده است.
او و پنج محقق آلزایمر دیگر نیز اظهار داشتند که این یک گزارش موردی میباشد نه یک مطالعه بزرگ. از سوی دیگر با توجه نادر بودن ژنهای این زن، ممکن است ثابت شود که ژن به ظاهر محافظ از ابتلای او به آلزایمر زودرس جلوگیری کرده است.
این زن (که نامش برای حفاظت از حریم خصوصی فاش نمیشود) به یک خانواده بزرگ کلمبیایی تعلق دارد. او از یک زوج باسکی متولد شده است که ۳۰۰ سال پیش به کلمبیا مهاجرت کردند و حدود ۱۲۰۰ نفر از هر ۶۰۰۰ نفر آنها دارای یک جهش ژنی به نام PSEN1 میباشند که در سال ۱۹۸۷ کشف شده است. این جهش (شناخته شده با عنوان E280A) باعث میشود که مغز به میزان بیشتری پروتئین بتا آمیلوئید تولید کند که پلاکهای چسبندهای را بین نورونها تشکیل میدهند و در کل نشانه اصلی تشخیص آلزایمر هستند (البته نه لزوماً علت بیماری).
از آن جا که خانوادههای کلمبیایی بزرگترین گروهی است که جهشهای عامل آلزایمر زودرس را در خودشان دارند – نیمی از افرادی که این ژن را دارا هستند تا سن ۴۴ سالگی به اختلال شناختی خفیف و در ۴۹ سالگی به زوال عقل مبتلا میشوند – از این رو آنها بخش مهمی از مطالعات بر روی این بیماری را شامل میشوند.
این زن در یکی از این مطالعات، مورد توجه عصب رواتشناسی به نام یاکیل کویروز از بیمارستان عمومی ماساچوست قرار گرفت. خانواده او گفتند که حافظه و تفکر این زن تا دهه ۵۰ و ۶۰ سالگی او وضعیت خوبی داشته است. هرچند تصویربرداری از مغز او نشان دهنده سطوح بسیار بالایی از آمیلوئید بود – همان طور که در صورت وجود ژن PSEN1 انتظار میرود – با این حال او فقط در ۷۰ سالگی یعنی سه دهه بعد از بستگان خودش که دارای جهش ژنتیکی PSEN1 بودند دچار اختلال شناختی خفیفی گردید.
در واقع پلاکهای آمیلوئید در او بیشتر از بستگان دیگرش بود و قدرت شناختی آنها در ۴۰ سالگی شروع به تحلیل رفتن نمود. او همچنین دارای سطوح نسبتاً پایینی از تاو در مغزش بود که قطعات پروتئینی هستند که در داخل نورونها اجتماع میکنند (و آنها را میکشند). او دچار تخریب عصبی (neurodegeneration) کمتری نیز شده بود.
کویروز و همکارانش برای این که دریابند این زن چطور از مبتلا شدن به آلزایمر زودرس نجات یافته است، ژنوم او را توالییابی کردند. یکی از ژنهای او با نام APOE3 بسیار غیرمعمول بود: هر دو کپی (یک مورد از مادرش و یک مورد از پدرش) دارای جهش نادری به نام “جهش کرایست چرچ” (Christchurch mutation) بودند که در سال ۱۹۸۷ در نیوزیلند کشف شده است. این جهش حدوداً در تمامی لاتین تبارها وجود دارد؛ گریسیوس استنفورد برآورد کرده است که از هر ۱۰۰ میلیون نفر تنها ۱ نفر هر دو کپی از این ژن را دارا هستند.
درست همانند هر انسان دیگری، این زن نیز دارای هزاران گونه ژنتیکی غیرمعمول میباشد. با این حال کویروز جهش کرایست چرچ را با توجه به الگوریتمی که انواع ژنها را برای بیماریهای خاص رتبهبندی میکند، تقریباً صفر در نظر گرفته است. اشکال مختلف APOE از مدتها پیش با آلزایمر ارتباط دارند: APOE4 ریسک ابتلا به این بیماری را افزایش میدهد، APOE2 ریسک ابتلا به بیماری را کاهش میدهد و APOE3 یک ژن خنثی میباشد (APOE1 وجود ندارد). کویروز گفت: این دلگرم کننده بود چرا که از نظر ما نوع کرایست چرچ APOE3، جالب بود.
او و تیمش برای تست کردن این احتمال بررسی کردند که چطور شکل کرایست چرچ در مولکولهای APOE3 با سایر مولکولهایی که در آلزایمر نقش دارند ارتباط برقرار میکند. فرم کرایست چرچ و همچنین نوع معمول APOE3 در ظروف آزمایشگاهی نتوانست به خوبی به مولکولهای قند (پروتئوگلیکانهای سولفات هپاران) متصل گردد. مطالعات قبلی نشان دادند که این قندها فعال کنندههای حیاتی برای تاو محسوب میشوند که آنها نیز به نوبه خود مولکولهای کشنده نورونها در آلزایمر میباشند: قندهایی که به APOE متصل میشوند باعث میشوند تا تاو از یک نورون به نورون دیگر پخش شده و با شعلههای سوزاننده خودش در محوطه مغز همانند یک آتش سوزی در جنگل باعث مرگ نورونها بشوند.
کویرز و تیمش به این نتیجه رسیدند که جهش کرایست چرچ، تشکیل و تجمع تاو و مرگ نورونها را حتی زمانی که مغز در آمیلوئید غرق شده است کاهش میدهد.
اگر نتیجه گیری آنها صحیح باشد، ممکن است داروهای آزمایشی برای پیشگیری یا درمان آلزایمر از شیوه بسیار متفاوتی نسبت به پاکسازی مغز از آمیلوئید استفاده کنند (که تقریباً در هیچ کدام از موارد نیز موفقیتی وجود نداشته است). کویروز و همکارانش نوشتند، ما در مقابل توانستیم آنتی بادی یا مولکولهایی را بسازیم که از اتصال APOE به قندهای پخش کننده تاو، حتی در افراد با ژنهای نرمال نیز جلوگیری میکنند. این کار میتواند تاثیر عمیقی بر درمان و پیشگیری از بیماری آلزایمر داشته باشد.
سایر دانشمندان چندان از این موضوع اطمینان نداشتند. شک اصلی: این بیمار نیز همانند سایر افراد، دهها هزار نوع ژن نادر دیگر نیز دارد که ممکن است یکی از آنها باعث شده باشد تا او به آلزایمر زودرس مبتلا نشود، درست همان طور که جهش PSEN1 باعث این اتفاق میشود.
نیکولاس روباکیس از دانشکده پزشکی ایکان در مونت سینای که یکی از اولین جهشها را برای آلزایمر زودرس کشف کرده است گفت: هزاران گونه مختلف (تنوع زیادی) در ژنوم ما وجود دارد. بنابراین بعید به نظر میرسد که بتوان به طور قاطع اظهار داشت که این همان دلیلی است که باعث شده این زن از سرنوشت ژنتیکی خودش فرار کند.
یکی از دلایل شک: گریسیوس از استنفورد اظهار داشت که داشتن یک کپی از ژن کرایست چرچ (همان طور که هفت نفر از ۱۱۷ عضو یک خانواده بزرگ دارا هستند) به جای داشتن دو کپی (که در این بیمار وجود داشت) ظاهراً هیچ سودی برای او ندارد. چهار نفر از این هفت نفر نیز دارای جهش آلزایمر زودرس بودند که همگی نیز به این بیماری مبتلا شدهاند.
او گفت قانع کنندهترین دلیل این است که نشان بدهیم دارا بودن دو کپی از ژن کرایست چرچ سن شروع بیماری را از اوایل دهه چهارم زندگی (چهل سالگی) به اوایل دهه هفتم (۷۰ سالگی) منتقل میکند و داشتن یک نسخه نیز سن ابتلا را به اوایل دهه ۵۰ زندگی منتقل کند. با این حال هیچ گونه اثر دوز (dose effect) در این رابطه وجود ندارد. به گفته روباکیس این یافتهها شواهدی علیه این ادعا هستند که این شکل نادر از APOE3 به عنوان یک جادوی ضد آلزایمر عمل میکند.
با این حال حتی افراد بدبین به این فرض نیز در یک مورد باهم اتفاق نظر داشتند: نقش APOE در آلزایمر به خوبی مورد مطالعه قرار نگرفته است. مورد مربوط به زن کلمبیایی توانست کمک ارزشمندی به تحقیقات آلزایمر بنماید.

