پلاکهای آمیلوئید در آلزایمر: خلق بهترین نتیجهٔ ممکن از یک موقعیت بد
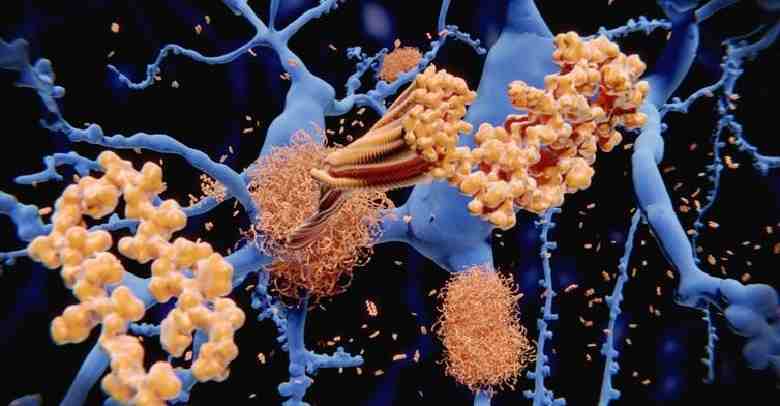
در بیماری آلزایمر، پلاکهای متراکم آمیلوئید در موشها، “از یک موقعیت بد بهترین نتیجۀ ممکن را خلق مینمایند”.
برای دهها سال، پلاکهای پروتئین آمیلوئید بتا هدف اصلی درمانهای بیماری آلزایمر بوده است، اما این داروها در کارآزماییهای بالینی مدام شکست میخورند. مطالعۀ جدیدی یک توضیح بالقوه ارائه مینماید.
این توضیح منوط به این حقیقت است که تمام پلاکهای آمیلوئید بتا یکسان خلق نمیشوند. برخی باریک و نازک هستند، و سایرین بهطور مناسبی پلاکهای هسته-متراکم نامگذاری میشوند.
گِرِگ لِمکه – استاد مؤسسۀ مطالعات بیولوژیکی سالک و نویسندۀ ارشد این تحقیق – میگوید: «این ایده وجود داشت که پلاکهای [هسته-متراکم] خود بخود شکل میگیرند؛ اما ضمن مطالعۀ نقش سلولهای ایمنی مغز در بیماری آلزایمر، گروه او دریافتند پلاکهای متراکم ممکن است بخشی از مکانیسم دفاعی مغز باشند.
مطالعات ژنتیک ارتباطهایی بین بیماری آلزایمر و ژنهای بیان شده در سلولهای ایمنی مغز بنام میکروگلیاها پیدا کردهاند. کارمِلا آبراهام، استاد بیوشیمی، داروشناسی و درمانهای آزمایشی در دانشکدۀ پزشکی دانشگاه بوستون، اظهار داشت: «نقش میکروگلیاها خلاص شدن از شر چیزهایی است که در مغز موردنیاز نیستند که سمی هستند.” آبراهام در این مطالعۀ جدید وارد نشد.
گروه لِمکه این پژوهش را شروع کردند تا با تمرکز بر دو گیرندۀ مهم بنامهای Axl و Mer، به نقش میکروگلیاها در مدلهای موشی بیماری آلزایمر نگاهی بیندازند. Axl و Mer به میکروگلیاها اجازه میدهند سلولهای در حال مردن در مغز را پاکسازی کنند. مطالعات پیشین نشان دادهاند Axl و Mer، که بخشی از یک گروه گیرندههای میکروگلیایی بنام TAM هستند، ممکن است نقشی در بیماری آلزایمر داشته باشند، اما نقشِ دقیق آنها مشخص نیست. به منظور پیبردن به آن، محققان دو گروه از موشهای دارای رسوب آمیلوئید در مغز را با هم مقایسه نمودند: یک گروه دارای میکروگلیاهای عملکردی و یک گروه بدون گیرندههای میکروگلیایی TAM.
وقتی محققان این مطالعه را آغاز کردند، تصور نمودند موشهای بدون گیرندههای TAM، نسبت به موشهای با میکروگلیاهای کاملاً عملکردی، دارای تجمع پلاک هسته-متراکم بیشتری خواهند بود. این بدان دلیل بود که دانشمندان فکر کردهاند میکروگلیاها، رشد پلاکهای آمیلوئید بتا را از طریق فراگرفتن این ماده محدود مینمایند.
یوتانگ هوآنگ، نویسندۀ اول این پژوهش و محقق فوقدکترا در مؤسسۀ مطالعات بیولوژیکی سالک، بیان داشت: “اما بهطور شگفتآوری، متوجه شدیم درواقع این موشهای فاقد TAM دارای بیماری آلزایمر، پلاکهای هسته-متراکم بسیار کمتری در قشر مغز و هیپوکامپ خود ایجاد کردند.” هیپوکامپ یک ساختار مغزی مهم برای حافظه است، و قشر مغز به لایۀ خارجی مغز اطلاق میشود که برای عملکردهایی مانند شناخت و پردازش اطلاعات حسی اهمیت دارد.
وقتی هوآنگ اولین بار دادههایش را به لِمکه نشان داد، وی متحیر گردید. او اندیشید،”این اصلاً معقول نیست.” در موشهای فاقد TAM، حذف آن گیرندهها مانع میکروگلیاها از بلعیدن مخروبههای سلولی، یعنی فرآیندی بنام فاگوسیتوز، گردید. اما بجای داشتن پلاکهای هسته-متراکم بیشتر، موشهای فاقد TAM نیمی از آن میزان را داشتند. اگر میکروگلیاها پلاکهای هسته-متراکم را در مغز پاکسازی مینمایند، آن نتایج معقول نبودند.
لِمکه اظهار نمود،”اما بعد وقتی واقعاً دیدیم که جریان از چه قرار است، این امر به این مدل که قطعی نیست ختم شد، که میکروگلیاها در حال ساختن پلاکهایی از طریق فاگوسیتوز هستند.” بهجای پاکسازی پلاکها، میکروگلیاها داشتند آنها را خلق میکردند. ایده این است که میکروگلیاها میتوانند، مانند یک دستگاه فشردهکنندۀ زباله، شکلهای زیانآورتر رسوب آمیلوئید بتا را مصرف کنند، و آن آمیلوئید بتا را خرد نموده و آن را به یک صورت فشرده شده، یعنی پلاکهای هسته-متراکم، رها نمایند.
با جمع کردن و کنار گذاشتن آمیلوئید بتا در این پلاکهای متراکم، میکروگلیاها آسیبی را که شکلهای سمیتر آمیلوئید بتا میتوانستند سبب شوند را ممکن است به حداقل برسانند. آبراهام فکر میکند این مدل معقول است. این امر ایدۀ قبلی را که پلاکهای هسته-متراکم ممکن است از سایر شکلهای آمیلوئید بتا کمتر زیانآور باشند، پشتیبانی مینماید.
و معلوم شد هر چند موشهای فاقد TAM، پلاکهای هسته-متراکم زیادی نداشتند، قطعاً دارای پلاکهای بیشتری به شکل پراکنده بودند. این پلاکهای بیقاعده بستهبندیشده، به گفتۀ لِمکه “پلاکهای اَبرمانند”، برخلاف پلاکهای هسته-متراکم، به طور حتم خودبخود شکل میگیرند. وی اظهار داشت،”و آنچه میکروگلیاها انجام میدهند این است که این چیزهای آزاد را فرامیگیرند و در وزیکولها میگذارند که آن را بسیار، بسیار، بسیار محکم میفشارند. آنگاه آن را به بیرون تف میکنند و در پلاکهای هسته-متراکم قرار میدهند.”
محققان، در موشهای فاقد TAM مشاهده نمودند آمیلوئید بتای بیشتری درون و اطراف رگهای خونی جمع شدند که میتواند اشاره به یک وضعیت رایج در بیماری آلزایمر، یعنی آنژیوپاتی آمیلوئید مغزی (CAA)، داشته باشد. این یافته در راستای مطالعات قبلی است که نشان دادند وقتی میکروگلیاها در موشها کم شدند، CAA افزایش یافت.
لِمکه، هوآنگ و همکارانشان نیز بافت مغز سه انسان دارای بیماری آلزایمر پیشرفته و سه مورد بدون آن را پس از مرگ بررسی نمودند. آنها شواهدی یافتند که گیرندههای TAM ممکن است نقش مشابهی را در انسانهای دچار بیماری آلزایمر ایفا کنند. بااین حال، مدل آزمایشی آنها تابحال فقط در مورد موشها کاربرد دارد.
آبراهام گفت،: «این امر، ما را بلافاصله به درمان نمیرساند.» هدف قراردادن این گیرندههای میکروگلیایی پیچیده است، و دانشمندان لازم است پی ببرند دستکاری آن گیرندهها چه اثراتی میتواند روی مغز انسان داشته باشد. وی افزود، «ما نمیخواهیم این توازن بسیار ملایم و حساس گیرندهها را تکان دهیم.»
یک محدودیت دیگر این است که مدلهای موشی آنها تنها یک مشخصۀ بیماری آلزایمر، یعنی پلاکهای آمیلوئید بتا، را انعکاس میدهند نه مشخصۀ دیگر، یعنی تودههای نوروفیبریلار پروتئین تائوی درون سلولها. هوآنگ بیان داشت: «نقش گیرندههای TAMو میکروگلیاها در پاتولوژی تائو، جنبۀ دیگری است که ما به آن علاقهمند هستیم. این یک بخش ناقص این مطالعه است.»
با این وجود، این مطالعه که در مجلۀ نیچر ایمونولوژی چاپ شد، توانست عدمموفقیت برخی درمانهای بیماری آلزایمر را توضیح دهد، مانند آنتیبادیهای طراحی شده جهت هدف قراردادن پلاکهای آمیلوئید بتای هسته- متراکم. لِمکه گفت: “آنتیبادیها موفقیت تأثیرگذاری در از هم پاشیدن پلاکها دارند.” اما آن امر به بهبود علایم تبدیل نمیشود. “آنها در واقع، به طور کلی، اثرات حاشیهای نسبی بر بهبود تواناییهای شناختی بیماران طی درمان شش ماهه تا یکساله دارند.”
آبراهام اظهار نمود این ممکن است بدان دلیل باشد که طبق مطالعۀ لِمکه و هوآنگ، “وقتی این آنتیبادیها منجر به تجزیۀ پلاکها میشوند، سمیترین شکل آمیلوئید بتا را از پلاکها آزاد میسازند.”
لِمکه هشدار میدهد، اما نمیگوییم پلاکهای هسته-متراکم برای مغز خوب هستند. “پلاکهای هسته-متراکم که شما در بیماری آلزایمر میبینید ممکن است تلاش بدن برای ایجاد بهترین نتیجه از یک موقعیت بد باشد.”

